Бензол – это широко используемое вещество и в промышленности, и в производстве сельскохозяйственных удобрений, и в бытовой химии, и даже в пищевой промышленности. На его основе выпускают и пищевые добавки: например, широко обсуждаемая E211 «бензоат натрия», которую некоторые относят к какой-то возбуждающей аппетит субстанции, а на самом деле она является консервантом. Бензол – это такое вещество, пользу от которого трудно переоценить. Пожалуй, без бензола и возможности его дополнительного синтеза наша современная жизнь никогда не была бы такой, какой она есть сейчас. Машины остались бы без моторных масел, пластмассы были бы непрочными и хрупкими, и даже производство печатных плат для компьютеров было бы невозможным.
Содержание
- Что такое бензол, формула, виды
- Физические свойства, внешний вид
- Формула бензола, химические свойства, уравнение
- Реакции с бензолом и его соединения и взаимодействия
- Производство и получение бензола
- Применение
- Воздействие на человека
- Опасность, токсичность, меры предосторожности
- Где купить и сколько стоит
- Заключение
Что такое бензол, формула, виды
Бензол – это циклический углеводород. То есть такое соединение, где углеводородные радикалы расположены замкнуто, начало молекулы соединено с её концом. Форма молекулы шестиугольная. Относится к ненасыщенным углеводородам, то есть не все внешние связи в атомах углерода соединены с внешними радикалами или водородом. Часть из них образует связи между собой.
Брутто формула бензола:
C6H6
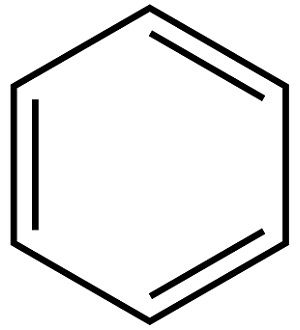
Шесть молекул углерода образуют внутреннее кольцо, к каждому из атомов углерода присоединён один атом водорода. Долгое время учёные считали, что часть связей в молекуле бензола двойные, а часть — одиночные. И представляли структурную формулу бензола так:
Однако эта структурная формула бензола вызывала ряд вопросов. Прежде всего, ни одна из химических реакций, характерных для других непредельных углеводородов, в том числе и циклических, не могла разорвать двойную связь между атомами углерода внутри молекулы. Все реакции, которые это пытались сделать, просто разрушали молекулу и она становилась нециклической. В то же время другие непредельные углеводороды обычно могут вступать в реакцию с разрывом двойной связи, сохраняя структуру молекулы.
В более позднее время учёные пришли к выводу, что молекула бензола не имеет стойких двойных связей — электроны во внутреннем кольце просто перетекают от одного атома к другому. Таким образом, двойные связи постоянно перемещаются, образуя кольцо внутри молекулы.
Впервые бензол был описан химиком Глаубером в своей книге, изданной в семнадцатом веке. Там он описывает бензолсодержащие субстанции, которые он получал при перегонки смолы из каменного угля. В чистом виде вещество было получено и описано химиком и физиком Майклом Фарадеем в 1825 году. Независимо от него бензол был получен химиком Эйльгардом Мичерлихом в 1833 году. Значительный вклад в исследование этого вещества внёс российский и советский химик Николай Зелинский. Современное промышленное получение бензола в основном происходит благодаря его методике комплексного катализа и нефтепереработки. Одна из реакций, при помощи которой получают бензол в промышленности, носит его имя.
Физические свойства, внешний вид
Чистый бензол является ядовитым химическим веществом, обычно находящимся в жидком состоянии. При комнатной температуре является бесцветной маслянистой жидкостью, имеющей резкий запах. Температура его плавления — 5.5°C, кипит при атмосферном давлении обычно при температуре 80.1° C. Бензол имеет меньшую плотность, чем вода, и плавает на её поверхности: его плотность 0.879 г/см3. Бензол имеет довольно большую молекулу — его молярная масса составляет 78.11 г/моль.
Вещество имеет хорошую растворимость в органических растворителях: диэтиловом эфире, бензине, керосине. В воде растворим хуже. При комнатной температуре растворимость в воде составляет всего лишь около 1.8 г/л. Имеет способность к горению при комнатной температуре: на воздухе горит ярким пламенем с образованием большого количества чёрного дыма. При испарении с воздухом образует смеси, которые могут привести к взрыву.
При охлаждении бензол образует аморфное соединение, не имеющее выраженной кристаллической решётки. Точно так же ведут себя, например, парафины, а также некоторые непредельные углеводороды. Молекула бензола может считаться идеальным плоским шестиугольником: атомы углерода в ней расположены строго по кольцу в одной плоскости, а связи от одного атома к другому направлены точно под углом 120°.
Температура вспышки бензола составляет -11°C. При этом температура самовоспламенения, та, при которой он способен поддерживать реакцию окислительного горения при обычных атмосферных условиях составляет в районе 560°C. Таким образом, хоть бензол и является горючим веществом, к классу особо огнеопасных или взрывоопасных его в чистом виде отнести нельзя. Тем не менее, он относится к классу легковоспламеняющихся жидкостей, и при его хранении нужно учитывать это условие: хранить в закрытой таре в отсутствии источников открытого огня, электрических разрядов, искр и других, способных вызвать воспламенение.
Бензол является веществом с небольшой вязкостью. Например, вода при комнатной температуре имеет вязкость примерно 1· 103Па·с. Бензол при этом имеет вязкость 0.635 · 103Па·с. Это свойство делает его довольно текучим. Например, он гораздо быстрее воды покинет пределы тары, в которой образовалась течь.
Формула бензола, химические свойства, уравнение
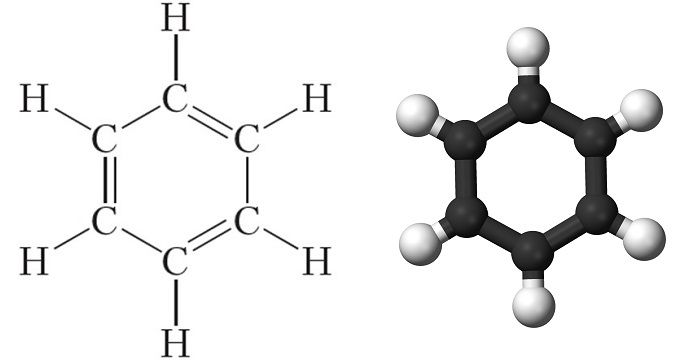
Химическая брутто-формула бензола – C6H6. Строение молекулы выглядит следующим образом:
В молекуле имеется шесть связей между атомами углерода, три двойных, образованных орбиталями SP2, и три одинарных. Двойные связи перемещаются по периметру молекулы непрерывно, размыкаясь и замыкаясь снова в новом месте. Имеется три внешних углеродных связи, которые заняты атомами водорода. В химических реакциях данные связи могут происходить с замещением на радикал, кислотный остаток или иную химическую группу. В ряде химических реакций двойные связи могут распадаться с сохранением гексагонального ядра молекулы и циклического строения.
Реакции с бензолом и его соединения и взаимодействия
Реакция горения бензола:
2C6H6 + 15O2 = 12CO2+6H2O+T
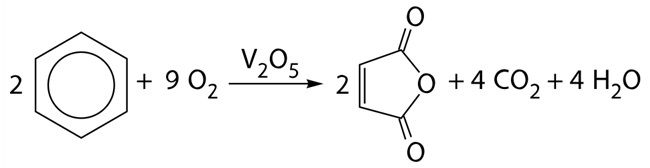
Существуют и другие реакции окисления бензола. Сам по себе бензол является устойчивым к окислению. Один из самых активных окислителей, перманганат калия, на него не действует. Тем не менее, реакция окисления может протекать в присутствии оксида ванадия:
В результате при окислении образуется малеиновый ангидрид.
Реакции замещения. Водород из внешних водородных связей замещается на радикал или остаток. Реакция проходит в многочисленных вариантах.
Получение хлорбензола:
C6H6 + Cl2 = C6H5Cl + HCl
Реакция идёт в присутствии катализатора, хлорида железа FeCl3.
В отсутствии катализатора данная реакция идёт с разрушением бензойного ядра и образованием гексахлорциклогексана:
C6H6 + 3Cl2 = C6H6Cl6
В данной реакции с образованием гексахлоргексана идёт превращение бензойного кольца в предельно насыщенное углеводородное кольцо. Углеродные связи из внутренних, двойных, переходят во внешние, соединяясь с хлором. Происходит это в значительной мере благодаря ионам хлора, которые оттягивают электроны из внутренних связей на себя. Молекула гексахлорциклогексана обладает стереометрической изомерией. В ходе реакции образуется смесь из изомеров, всего возможных стереомеров шесть штук.
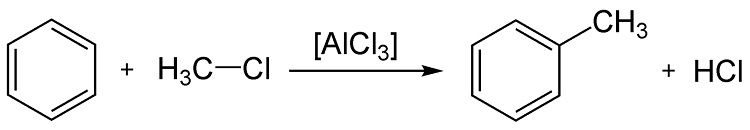
Реакция с галогенопарафинами и образованием метилбензола:
В некоторых случаях, зависит от исходного сырья, в ходе этой реакции удаётся получить диметилбензол. Триметилбензол на практике удаётся получить в основном при пиролизе нефтепродуктов. Метилбензолы различного рода носят общее название толуол. Реакция носит название Фиделя — Крафтса.
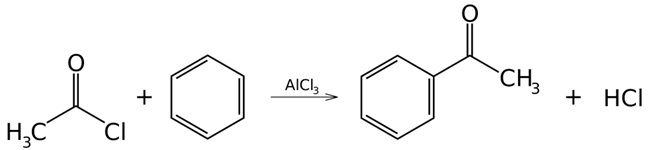
Схожим образом проходит реакция по механизму Фиделя-Крафтса при взаимодействии с ангидридами различных кислот:
Взаимодействие происходит с образованием кислоты, в данном случае соляной. Может происходить и с другими радикалами. Обе описанные реакции с соляной кислотой и её ангидридом идут в присутствии катализатора хлорид алюминия.
Производство и получение бензола
Основной способ получения бензола — его выделение из нефтяных фракций, в частности, бензиновых. В США этим способом его производится около 80%, в Европе — до 60%. Традиционный способ получения бензола, описанный ещё химиком Глаубером — получение при коксовании каменного угля. С его помощью получается сравнительно небольшое количество — около 10% во всём мире. Всё дело из-за примесей, которые при этом образуются — тиофена, и присутствия в каменном угле серы, вступающей в реакцию.
Химически чистый бензол, который используют в парфюмерии, при производстве ракетного топлива, в других реакциях, получают при помощи реакции Зелинского. Получение бензола этим способом:
3C2H2 = C6H6 (T, K)
Реакция проходит в присутствии катализатора — активированного угля, и при температуре 400°C. Строго говоря, реакцию тримеризации ацетилена открыл не Зелинский. Она впервые была проведена и до него рядом химиков, в частности, Бертоло, Реппе, однако реакция Бертоло проходила с выделением большого количества примесей. Окончательно реакцию тримеризации ацетилена удалось детально описать только в 2020 году после ряда исследований Института имени Зелинского.
Наконец, некоторую часть бензола производят при помощи пиролиза тяжёлой фракции нефти. В данном случае есть возможность получения бензола и толуола, а также ряда других бензоалканов в составе продуктов реакции.
Применение
Применение бензола распространяется чуть ли не на все сферы жизни современного человека. Большая часть бензола, производимого в мире, используется в качестве реагента при производстве пенополистирольного пластика. Некоторая часть идёт также для производства обычного пластика на основе стиролов – гранул, которые используются при производстве изделий на термопластавтоматах. Вторая сфера применения бензола — это превосходное сырьё-полуфабрикат, применяющееся практически во всех сферах жизнедеятельности человека. Благодаря применению бензола, например, стало возможным производство следующих продуктов:
- Анилиновых красителей — бензол основное сырьё для производства анилина;
- Фенола — компонента для производства многочисленной группы ядохимикатов и других изделий;
- Синтетических смол. В основном их производство ведётся на сырье из бензола и некоторых других реагентов. Синтетические смолы — неотъемлемая компонента фанеры, древесных плит, которые нужны для производства мебели и строительства.
- Различных растворителей, лаков и красок. Без применения бензола невозможно было бы производство лаков для ногтей, полиграфической продукции, где активно используются стойкие к истиранию и практичные красители.
- Парфюмерная и косметическая продукция. Применение бензола происходит практически везде, где есть синтетическая составляющая в косметике или духах. Без бензола производство их было бы невозможно.
- Применение бензола в освоении космоса. Анилин, который нужен для топлива космических ракет, получают из бензола.
- Лекарственные средства — их производство было бы невозможно без сырья на основе бензола.
- Производство инсектицидов. Легендарный препарат ДДТ в своём составе молекулы имеет целых две циклических бензойных группы.
- Производство бутадиен-стирольного каучука. Бензол является необходимым компонентом для его синтеза и входит в состав молекулы мономера.
Мы видим, что искусственно полученная органическая молекула бензола настолько изменила нашу жизнь, что, несмотря даже на многие негативные свойства этого вещества, отказаться от него означает фактически откатить наш быт назад на несколько столетий. Применение бензола осуществляется во многих сферах деятельности человека.
Воздействие на человека
Бензол является ядовитым канцерогенным веществом. В то же время химические соединения бензола могут и не проявлять негативных свойств. Самую большую опасность представляет попадание бензола внутрь человеческого организма через пищеварительный тракт. А также вдыхание его паров — так он способен быстрее всасываться в кровь, но при этом количество поглощённого вещества будет меньше. Представляет опасность попадание на кожу, в глаза, на слизистые оболочки носа, половых органов, а также слизистую внутренних органов даже в небольших количествах.
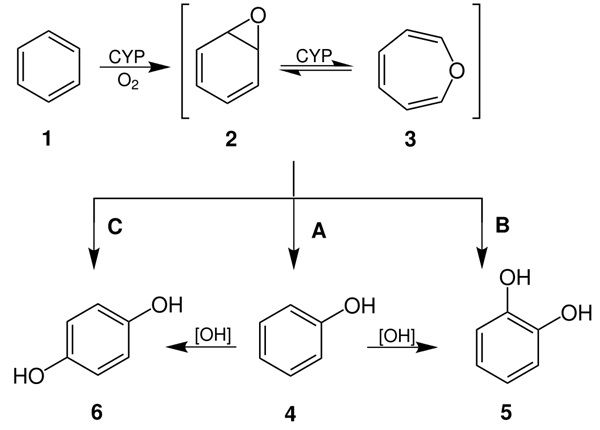
На картинке ниже изображены превращения бензола в человеческом организме с образованием токсичных веществ.
Бензол – это вещество, которое воздействует на организм человека, схоже с воздействием радионуклеидов, особенно при хроническом отравлении.
Отравление бензолом
Принято различать острое и хроническое отравление бензолом. В медицинской практике оба случая встречаются с одинаковой частотой. Они, в основном, бывают у людей, которые работают на химических производствах, на работе в сельском хозяйстве при обработке полей, а также у людей, использующих соединения бензола для токсикомании. Схожие симптомы отравления проявляет не только чистый бензол, но и его соединения с углеводородными радикалами, например, толуол. Отравление толуолом встречается и в быту, например, при автомалярных работах, проводящихся с нарушением правил техники безопасности. Токсическое действие в основном выражается в поражении внутренних органов, центральной нервной системы, а также угнетении кроветворения.
Острое отравление
Острое отравление принято делить на три степени:
- лёгкое;
- среднее;
- тяжёлое.
Тяжёлое отравление считается самым опасным, при нём почти мгновенно наступает потеря сознания. Человек погружается в токсическую кому, при которой он не может поддерживать жизнедеятельность в нормальном состоянии. Почти всегда в случае тяжёлого острого отравления наступает смерть. Такое отравление обычно возникает, если человек принимает бензол внутрь.
Острое отравление средней тяжести обычно проходит через несколько дней без тяжёлых последствий для человеческого организма. В некоторых случаях наступает стойкое нарушение работы центральной нервной системы, вегетативное расстройство астенического типа. Симптомы отравления средней тяжести:
- Снижение температуры тела;
- Падение артериального давления;
- Пульс частый;
- Появляется неадекватность в поведении, беспокойство;
- Расширение зрачков, судороги, тремор;
- Есть вероятность потери сознания;
- Кратковременный умеренный лейкоцитоз без глубоких поражений кроветворных функций костного мозга;
- Головная боль и слабость.
Прогноз после отравления средней тяжести, как правило, благоприятный.
Лёгкое отравление бензолом характеризуется следующими симптомами:
- Головная боль и слабость;
- Выраженное пошатывание при ходьбе;
- Тошнота, рвота;
- Шум в ушах.
При лёгком отравлении симптомы нестойкие и проходят уже через 5-6 часов. Тем не менее, необходимо наблюдение у врача.
В случае контакта с веществом необходимо пострадавшего немедленно удалить из зоны поражения. Отравление может произойти как от вдыхания паров, так и от попадания на кожу и слизистые оболочки. При попадании на слизистые необходимо по возможности промыть их физраствором или водой. Точно так же при попадании на кожу следы бензола необходимо смывать. Для этого используется мыльная вода. Одежду, если она была загрязнена, необходимо немедленно удалить. Сразу же необходимо вызвать врача.
После этого пострадавшего нужно уложить и оказывать ему медицинскую помощь — как правило, это симптоматическое лечение, например, принести воды, укрыть. Давать какие-то специализированные препараты запрещено. В случае, если пострадавший потерял сознание, нужно проводить реанимационные мероприятия до приезда врача: делать искусственное дыхание и непрямой массаж сердца.
Хроническое отравление
Обычно возникает в случае систематического попадания на кожу небольших доз, а также при постоянном вдыхании в небольшом количестве паров бензола. Выражается в нарушении функции кроветворения, также в нарушении функций печени и головного мозга. Выявить отравление можно при помощи анализа крови. Обычно в случае не слишком длительного воздействия сразу можно обнаружить нарушение при анализе крови: сниженное количество лейкоцитов. Затем, при более длительном воздействии происходит уменьшение количества тромбоцитов, и при ещё более длительном — образование эритроцитов.
В случае хронического отравления необходимо выявить причину, по которой бензол контактирует с организмом, и устранить её. В дальнейшем нужно проводить мероприятия по детоксикации под наблюдением врача-специалиста. Следы бензола при разных степенях отравления находят в головном мозге, костном мозге и печени.
Мутагенные и канцерогенные свойства бензола
Бензол относится к чрезвычайно опасным веществам при длительном воздействии на человеческий организм. Мутагенные и канцерогенные свойства бензола достоверно доказано. Бензол – это одно из немногих веществ, канцерогенное действие которого точно доказано многочисленными медицинскими исследованиями. В частности, некоторые учёные относят его к первому классу опасности по воздействию на репродуктивную систему человека, а также на повышение вероятности возникновения рака различной паталогии. Также не следует забывать о накопительных свойствах бензола – это вещество, которое обладает способностью накапливаться в организме и довольно медленно выводится.
Основная опасность воздействия бензола заключена в том, что он способствует возникновению мутаций при делении клеток. Доказано, что люди, у которых было хроническое отравление бензолом, чаще страдают астмой, аутоиммунными заболеваниями, такими, как сахарный диабет, аутоиммунный тиреодит. Воздействие оказывается в том числе и на нервную систему.
Бензол может накапливаться в костном мозге. Токсины такого рода выводятся из организма достаточно сложно и долго. Из-за его мутагенного воздействия могут возникать осложнения в развитии плода. У родившегося ребёнка чаще возникают паталогии, чем у того, который родился у пары, не подвергавшейся воздействию токсина.
Канцерогенные свойства бензола также довольно опасны. Он вызывает различные виды рака, прежде всего — рак крови. Эти виды заболевания труднее всего поддаются лечению, как правило, неоперабельны. Прогноз при их возникновении обычно всегда отрицательный.
Токсикомания бензолом
В чистом виде бензол, ввиду его отсутствия в широкой розничной продаже, для токсикомании не употребляется. Однако его соединения, например, толуол, растворители, могут использоваться в этих целях. При попадании паров толуола в лёгкие наблюдаются примерно те же симптомы, что и при лёгком отравлении бензолом: головокружение, спутанность сознания, расширение зрачков. При тяжёлом отравлении может наступать потеря сознания.
Сам бензол в наркоторговле не играет какой-то существенной роли. Однако некоторые его соединения, например, бензальдегид, находятся в списке веществ, которые законодательство РФ относит к прекурсорам для получения наркотических веществ. Наряду с ангидридом уксусной кислоты, он используется для получения ацетилированного опия, героина, из содержащих опий препаратов: некоторых лекарственных средств, маковой соломки или опия-сырца. Бензол может выступать в роли прекурсора при производстве некоторых других видов токсичных наркотических средств.
Опасность, токсичность, меры предосторожности
При транспортировке бензол необходимо держать в плотно закрытой таре. Так как он относится к классу легковоспламеняющихся жидкостей, необходимо беречь его от контакта с источниками высокой температуры, очагов пламени и избегать электроразряда в непосредственной близости с ним. Для хранения в небольших количествах используется обычно стеклянная тара с соответствующей маркировкой. Для больших объёмов применяют тару из нержавеющей стали. Хранить в пластиковой таре его нельзя, так как он с некоторыми видами пластика способен взаимодействовать, уменьшая их прочность и растворяя со временем стенку.
При работе с бензолом обязательно используют защитные средства: противогаз и защитный костюм. В случае работы с небольшими объёмами вещества допускается применять только респиратор и защитные перчатки. При этом ряд защитных средств не допускается использовать из-за того, что возможно появление искры во время работы от статического электрического разряда. Это может привести к возгоранию паров бензола. Обязательно наличие вытяжки при проведении лабораторных опытов с бензолом.
Какое-то производство с использованием бензола в качестве реагента или катализатора обязательно должно проходить проверку и сертификацию в органах охраны труда, организовывать его без такого разрешения не допускается. Точно также нельзя без согласования с органами охраны труда и экологической безопасности проводить какие-то работы по утилизации бензола — например, мытью химической тары, вагонов, цистерн.
Где купить и сколько стоит
Опасные свойства бензола обусловили невозможность покупки больших количеств вещества в свободной продаже. Обычно раствор бензола в небольших количествах можно купить в специальных магазинах, торгующих химическими реактивами. Тара объёмом до литра раствора бензола чаще всего идёт стеклянная, бутылка из тёмного стекла с закручивающейся пробкой. Тара большего объёма, двадцать или сорок литров раствора бензола, уже идёт металлическая. Соответственно, при покупке раствора бензола придётся также оплачивать и стоимость тары.
Цена раствора бензола будет зависеть и от стоимости тары, в которой он приобретается, и от объёмов закупаемого вещества. В небольшой бутылке он обойдётся в районе 300-400 российских рублей за литр. При увеличении объёма цена за литр будет расти, главным образом за счёт стоимости тары. Например, за кану 40 литров раствора бензола придётся заплатить уже порядка 15 тысяч рублей. Если покупать уже промышленными объёмами, то цена за литр начинает снижаться.
Заключение
Бензол – это вещество, без которого невозможна была бы современная жизнь. С его помощью можно построить дом, сделать лекарство, запустить ракету в космос. В то же время канцерогенные и мутагенные свойства бензола таят опасность, это ядовитое вещество. Бензол требует осторожного обращения при транспортировке и складировании — он горюч и ядовит.
Читайте также:


























Оставить комментарий